弊社及び当社ウェブサイトに関する
お問い合わせはこちら。
 rodanius for Pharma
rodanius for Pharma
医薬製薬業界に特化したQC支援ツール:
自動文書突合・正誤判定ソリューション。
QC業務の時間を短縮し、正確な文書作成を支援します。
QCチェック:文書間の一貫性担保が必要な
すべての部門で活用可能です。
承認申請書類、添付文書、試験報告書、GMP文書、GVP文書、GCP文書、手順書など
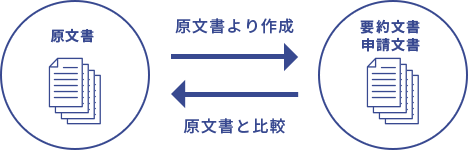
作成文書の記載内容は
一致させなければならない
- 該当箇所を探すのが大変
齟齬がないようにするのが大変
どの書類をもとにしているのか探すのが大変
・・・ 確認作業が膨大で、ダブルチェックなど
多くの工数を要する
rodanius for Pharma が解決!
社外文書(申請文書等)と原文書(製造指図書、試験指図書等)の不一致箇所を検出します。
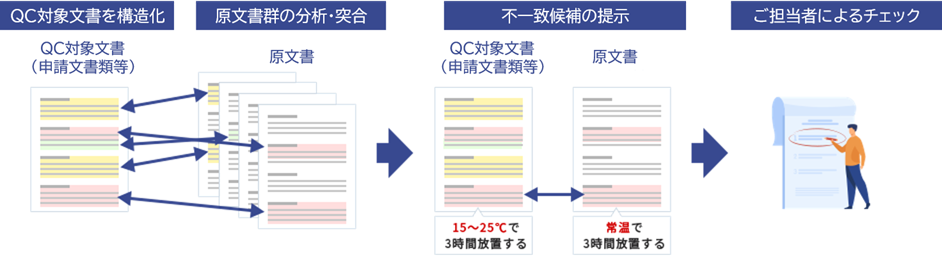
活用事例:GMP関連文書の齟齬チェック
2021年施行された改正GMP省令で、規定された多数の文書・記録の作成保管が義務付けられており、文書作成の際には、Data Integrity(完全性)の確保が求められています。
関係部署
- GMPの資料作成
- 品質保証管掌部署(品質保証部、グループ品質保証・環境安全部など)
- 原資料作成
- 製造管掌部署(生産本部、製薬技術本部各工場、グループ会社の各工場など)
対象となる文書
- GMP適合性調査申請書
- 製品標準書
- 製品製造仕様書
- 製造指図書(MBR)・製造記録
- 標準操作手順書(SOP) など
GMP申請時の関連文書間
の齟齬確認
Data Integrity(完全性)
の確保
活用事例:その他
- 承認申請書類と各関連原文書の記載内容の一致性
- 再審査申請書、安全性定期報告書、使用成績調査
- 総合製品情報概要の校正、改訂箇所の確認
- 医療機関向けお知らせ文書、疾患解説資材、患者向けリーフレット、冊子などの校正、改訂箇所の確認
- 資材研修用資材の校正、改訂箇所の確認
- Web講演会資料(プレゼンテーション資料)の校正、改訂箇所の確認
- その他文書のQC業務
PoCから技術実現性を検証し、導入~開発・運用まで提供いたします。
まずはお問い合わせください。
POC
- 期間:3カ月
- 要件定義
- sampleデータ受領
- PoC検証
- 定例会
- PoC結果報告
初期導入
- 期間:要件により変動
- 環境構築
- 初期チューニング
- ※期間は取込文書数に
応じて変動します。
運用
- 契約形態:年間契約
- 運用保守
- サポート
- 商用化フェーズ
- ※PoCとは、Proof of Conceptの略で、「概念実証」という意味です。
新しい概念や理論、原理、アイディアの実証を目的とした、試作開発の前段階における検証やデモンストレーションを指します。
CONTACT US
当社製品に関する
お問い合わせはこちら。
採用に関する
お問い合わせはこちら。


